b) Trộn 8ml dung dịch H2SO4 0,7M với 12 ml dung dịch NaOH trong một bình B. Cho giấy quỳ vào bình B thấy có màu xanh. Sau đó thêm từ từ dung dịch HCl 0,05M vào bình B tới khi giấy quỳ đổi thành màu tím thì thấy hết 40ml dung dịch axit. Tính nồng độ mol của dung dịch NaOH.

Những câu hỏi liên quan
Trộn 8ml dung dịch H2SO4 0,7M và 12ml dung dịch NaOH trong bình B . Cho giấy quỳ vào bình B thấy có màu xanh . Sau đó thêm từ từ dung dịch HCl 0,05M vào bình B tới khi giấy quỳ đổi thành màu tóm thì thấy hết 40ml dd axit.
tính nồng độ mol của dd NaOH
H2SO4 + 2NaOH--> Na2SO4 + 2H2O(1)
Do sau PỨ quỳ chuyển xanh => NaOH dư
NaOH + HCl--> NaCl + H2O(2)
sau PỨ chuyển tím => PỨ hoàn toàn
TA có nH2SO4=0,7.0,008=0,0056=nNaOH(1)
nHCl=0,05.0,04=0,002=nNaOH(2)
=> CM ddNaOH= (0,0056+0,002)/0,012=0,63M
Đúng 0
Bình luận (2)
Có 2 dung dịch H2SO4 (dung dịch A) và NaOH (dung dịch B)
TN1: Trộn 0,2 lít dung dịch A với 0,3 lít dung dịch B được 0,5 lít dung dịch C. Lấy 20ml dung dịch C, thêm 1 ít quỳ tím vào thấy có màu xanh. Sau đó thêm từ từ dung dịch HCl 0,05M tới khi quỳ trở thành màu tím thấy hết 40ml dung dịch axit
TN2: Trộn 0,3 lít dung dịch A với 0,2 lít dung dịch B được 0,5 lít dung dịch D. Lấy 20ml dung dịch D, thêm 1 ít quỳ tím vào thấy có màu đỏ. Sau đó thêm từ từ dung dịch NaOH 0,1M tới khi quỳ trở thành màu...
Đọc tiếp
Có 2 dung dịch H2SO4 (dung dịch A) và NaOH (dung dịch B) TN1: Trộn 0,2 lít dung dịch A với 0,3 lít dung dịch B được 0,5 lít dung dịch C. Lấy 20ml dung dịch C, thêm 1 ít quỳ tím vào thấy có màu xanh. Sau đó thêm từ từ dung dịch HCl 0,05M tới khi quỳ trở thành màu tím thấy hết 40ml dung dịch axit TN2: Trộn 0,3 lít dung dịch A với 0,2 lít dung dịch B được 0,5 lít dung dịch D. Lấy 20ml dung dịch D, thêm 1 ít quỳ tím vào thấy có màu đỏ. Sau đó thêm từ từ dung dịch NaOH 0,1M tới khi quỳ trở thành màu tím thấy hết 80ml dung dịch NaOH. a/ Tính CM của 2 dung dịch A và B b/ Trộn VB lít dung dịch NaOH và VA lít dung dịch H2SO4 ở trên thu được dung dịch E. Lấy Vml dung dịch E cho tác dụng với 100ml dung dịch BaCl2 0,15M được kết tủa F. Mặt khác , lấy Vml dung dịch E cho tác dụng với 100ml dung dịch AlCl3 1M được kết tủa G. Nung F hoặc G ở nhiệt độ cao đến khối lượng không đổi thì thu được 3,262 chất rắn. Tính tỉ lệ VB:VA
Có hai dung dịch; H4 (dung dịch A), và NaOH (dung dịch B). Trộn 0,2 lít dung dịch A với 0,3 lít dung dịch B được 0,5 lít dung dịch C.
Lấy 20 ml dung dịch C, thêm một ít quì tím vào, thấy có màu xanh. Sau đó thêm từ từ dung dịch HCl 0,05M tới khi quì tím đổi thành màu tím thấy hết 40 ml dung dịch axit.
Trộn 0,3 lít A với 0,2 lít B được 0,5 lít dung dịch D. Lấy 20 ml dung dịch D, thêm một ít quì tím vào thấy có màu đỏ. Sau đó thêm từ từ dung dịch NaOH 0,1M tới khi quì tím đổi thành màu tím thấy...
Đọc tiếp
Có hai dung dịch; H4 (dung dịch A), và NaOH (dung dịch B). Trộn 0,2 lít dung dịch A với 0,3 lít dung dịch B được 0,5 lít dung dịch C.
Lấy 20 ml dung dịch C, thêm một ít quì tím vào, thấy có màu xanh. Sau đó thêm từ từ dung dịch HCl 0,05M tới khi quì tím đổi thành màu tím thấy hết 40 ml dung dịch axit.
Trộn 0,3 lít A với 0,2 lít B được 0,5 lít dung dịch D. Lấy 20 ml dung dịch D, thêm một ít quì tím vào thấy có màu đỏ. Sau đó thêm từ từ dung dịch NaOH 0,1M tới khi quì tím đổi thành màu tím thấy hết 80 ml dung dịch NaOH.
a. Tính nồng độ mol/l của 2 dung dịch A và B.
b. Trộn VB lít dung dịch NaOH vào VA lít dung dịch H2SO4 ở trên ta thu được dung dịch E. Lấy V ml dung dịch E cho tác dụng với 100 ml dung dịch BaCl2 0,15 M được kết tủa F. Mặt khác lấy V ml dung dịch E cho tác dụng với 100 ml dung dịch AlCl3 1M được kết tủa G. Nung F hoặc G ở nhiệt độ cao đến khối lượng không đổi thì đều thu được 3,262gam chất rắn. Tính tỉ lệ VB:VA
a. PTHH:
+ Lần thí nghiệm 1: 2NaOH + H2SO4 → Na2SO4 + 2H2O (1)
Vì quỳ tím hóa xanh, chứng tỏ NaOH dư. Thêm HCl:
HCl + NaOH → NaCl + H2O (2)
+ Lần thí nghiệm 2: phản ứng (1) xảy ra, sau đó quỳ hóa đỏ chứng tỏ H2SO4 dư. Thêm NaOH:
2NaOH + H2SO4 → Na2SO4 + 2H2O (3)
+ Đặt x, y lần lượt là nồng độ mol/l của dung dịch A và dd B: Từ (1),(2),(3) ta có:
0,3y - 2.0,2x = 0,05 (I)
0,3x - \(\dfrac{0,2y}{2}\) = 0,1 (II)
Giải hệ (I,II) ta được: x = 0,7 mol/l , y = 1,1 mol/l
b, Vì dung dịch E tạo kết tủa với AlCl3 , chứng tỏ NaOH còn dư.
AlCl3 + 3NaOH → Al(OH)3 + 3NaCl (4)
2Al(OH)3 → Al2O3 + 3H2O (5)
Na2SO4 + BaCl2 → BaSO4 + 2NaCl (6)
Ta có n(BaCl2) = 0,1.0,15 = 0,015 mol
n(BaSO4) = 3,262 : 233= 0,014 mol < 0,015 mol
⇒ n(H2SO4) = n(Na2SO4) = n(BaSO4) = 0,014 mol . Vậy VA = 0,014 : 0,7 = 0,02 lít
n(Al2O3) = 3,262 : 102 = 0,032 mol và n(AlCl3) = 0,1.1 = 0,1 mol.
+ Xét 2 trường hợp có thể xảy ra:
- Trường hợp 1: Sau phản ứng với H2SO4,NaOH dư nhưng thiếu so vời AlCl3 (ở pư (4): n(NaOH) pư trung hoà axit = 2.0,014 = 0,028 mol
nNaOH pư (4) = 3n(Al(OH)3) = 6n(Al2O3) = 6.0,032 = 0,192 mol.
Tổng số mol NaOH bằng 0,028 + 0,192 = 0,22 mol
Thể tích dung dịch NaOH 1,1 mol/l là \(\dfrac{0,22}{1,1}\)= 0,2 lít . Tỉ lệ VB : VA = 0,2 : 0,02 = 10
- Trường hợp 2: Sau (4) NaOH vẫn dư và hoà tan một phần Al(OH)3:
Al(OH)3 + NaOH → NaAlO2 + 2H2O (7)
Tổng số mol NaOH pư (3,4,7) là: 0,028 + 3.0,1 + 0,1 - 2.0,032 = 0,364 mol
Thể tích dung dịch NaOH 1,1 mol/l là \(\dfrac{0,364}{1,1}\)= 0,33 lít
⇒ Tỉ lệ VB : VA = 0,33 : 0,02 = 16,5
Đúng 2
Bình luận (0)
Có hai dung dịch; H2SO4 (dung dịch A), và NaOH (dung dịch B). Trộn 0,2 lít dung dịch A với 0,3 lít dung dịch B được 0,5 lít dung dịch C.Lấy 20 ml dung dịch C, thêm một ít quì tím vào, thấy có màu xanh. Sau đó thêm từ từ dung dịch HCl 0,05M tới khi quì tím đổi thành màu tím thấy hết 40 ml dung dịch axit.Trộn 0,3 lít A với 0,2 lít B được 0,5 lít dung dịch D. Lấy 20 ml dung dịch D, thêm một ít quì tím vào thấy có màu đỏ. Sau đó thêm từ từ dung dịch NaOH 0,1M tới khi quì tím đổi thành màu tím thấy h...
Đọc tiếp
Có hai dung dịch; H2SO4 (dung dịch A), và NaOH (dung dịch B). Trộn 0,2 lít dung dịch A với 0,3 lít dung dịch B được 0,5 lít dung dịch C.
Lấy 20 ml dung dịch C, thêm một ít quì tím vào, thấy có màu xanh. Sau đó thêm từ từ dung dịch HCl 0,05M tới khi quì tím đổi thành màu tím thấy hết 40 ml dung dịch axit.
Trộn 0,3 lít A với 0,2 lít B được 0,5 lít dung dịch D. Lấy 20 ml dung dịch D, thêm một ít quì tím vào thấy có màu đỏ. Sau đó thêm từ từ dung dịch NaOH 0,1M tới khi quì tím đổi thành màu tím thấy hết 80 ml dung dịch NaOH.
a. Tính nồng độ mol/l của 2 dung dịch A và B.
b. Trộn VB lít dung dịch NaOH vào VA lít dung dịch H2SO4 ở trên ta thu được dung dịch E. Lấy V ml dung dịch E cho tác dụng với 100 ml dung dịch BaCl2 0,15 M được kết tủa F. Mặt khác lấy V ml dung dịch E cho tác dụng với 100 ml dung dịch AlCl3 1M được kết tủa G. Nung F hoặc G ở nhiệt độ cao đến khối lượng không đổi thì đều thu được 3,262 gam chất rắn. Tính tỉ lệ VB:VA
Bạn nên chia nhỏ câu hỏi ra nhé để mn đỡ ngại làm bài :))
Đúng 3
Bình luận (7)
Chất tác dụng với dung dịch HCl tạo thành chất khí nhẹ hơn không khí là:
A: Na2SO3
B:CaCO3
C:MgCO3
D:Mg
Câu2:cho mẩu quỳ tím vào dung dịch NaOH. Thêm từ từ dung dịch HCl vào cho đến dư ,ta thấy mẩu giấy quỳ
A: màu đỏ. B. Màu đỏ chuyện dần sang xanh
Bài 1: câu D(Sinh ra H2 nhẹ hơn không khí)
Câu 2:A do thêm đến khi HCl dư,tức là dd có tính axit->quỳ tím đổi màu đỏ
Đúng 0
Bình luận (0)
Cho dung dịch có chứa 12 gam NaOH phản ứng với dung dịch chứa 29,4 gam H2SO4. Sau phản ứng thu được dung dịch X. Thử giấy quỳ tím với dung dịch X thấy giấy quỳ tím chuyển sang màu A. Đỏ. B. Xanh. C. Tím. D. Vàng
Đọc tiếp
Cho dung dịch có chứa 12 gam NaOH phản ứng với dung dịch chứa 29,4 gam H2SO4. Sau phản ứng thu được dung dịch X. Thử giấy quỳ tím với dung dịch X thấy giấy quỳ tím chuyển sang màu
A. Đỏ. B. Xanh. C. Tím. D. Vàng
\(n_{NaOH}=\dfrac{12}{40}=0,3\left(mol\right);n_{H_2SO_4}=\dfrac{29,4}{98}=0,3\left(mol\right)\\ PTHH:2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\\ Vì:\dfrac{0,3}{2}< \dfrac{0,3}{1}\Rightarrow H_2SO_4dư\)
=> Quỳ tím hoá đỏ
=> CHỌN A
Đúng 0
Bình luận (0)
Cho 10,0 ml dung dịch NaOH 0,1M vào cốc đựng 15,0 ml dung dịch HCl 0,1M. Dung dịch tạo thành sẽ làm cho
A. phenolphtalein không màu chuyển thành màu hồng. C. giấy quỳ tím hóa đỏ.
B. phenolphtalein không màu chuyển thành màu xanh. D. giấy quỳ tím không chuyển màu.
\(n_{OH^-}=0,01.0,1=0,001\left(mol\right)\)
\(n_{H^+}=0,015.0,1=0,0015\left(mol\right)\)
\(\Rightarrow n_{H^+dư}=0,0005\left(mol\right)\)
\(\Rightarrow\left[H^+\right]=\dfrac{0,0005}{0,01+0,015}=0,02\left(mol\right)\)
\(\Rightarrow pH\approx1,7\)
\(\Rightarrow\) Quỳ tím hóa đỏ.
Đúng 2
Bình luận (0)
Đổ dung dịch chứa 1g HBr vào dung dịch chứa 1g NaOH. Nhúng giấy quỳ tím vào dung dịch thu được thì giấy quỳ tím chuyển sang nàu nào sau đây:
A. Màu đỏ.
B. Màu xanh.
C. Không đổi màu.
D. Không xác được.
B đúng.
nHBr = 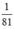 mol
mol
nNaOH = 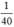 mol
mol
NaOH + HBr → NaBr + H2O
nNaOH > nHBr (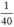 >
> 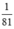 ) ⇒ sau phản ứng NaOH dư
) ⇒ sau phản ứng NaOH dư
⇒ nhúng giấy quỳ vào dung dịch thu được giấy quỳ sẽ chuyển màu xanh
Đúng 0
Bình luận (0)
trộn 50 ml dung dịch A với 100 ml dung dịch B được dd D .cho quỳ tím vào dd D thấy có màu xanh.thêm từ từ 20ml hcl 0,1M vào dd D thấy quỳ tím trở lại màu tím: tính nồng độ mol của các dd A, B






























